Влияние контакта разнородных металлов
При контакте двух разнородных металлов в общем электролите возникает макрокоррозионный гальванический элемент , вкотором более отрицаткльный металл играет роль анода, более положительный - катода ( см рис. 1.13). Контактная коррозия возникает:
а) в изделиях, состоящих из двух разнородных металлов с большей разницей потенциалов ( больше 0,5В)
б) в местах соединений, выполненных с помощью металлов или сплавов разного состава
в) в изделиях, изготовленных из одного металла, но находящегося в различных состояниях ( отжиг, закалка и др.), или имеющего другие неоднородности
г) в электролитах, окислительные ионы которых более положительны, чем металл изделия, например железо или алюминий в растворах медных солей. В этом случае контакт возникает в результате отложения металлической меди ( из раствора) на стальном изделии.
Потенциалы металлов в различных электролитах не одинаковы. Поэтому интенсивность контактной коррозии зависит не только от природы контактирующих металлов , но и от электролита. В табл. 1.3 приведены знаяения потенциалов некоторых металлов в типичных электролитах.
а) в изделиях, состоящих из двух разнородных металлов с большей разницей потенциалов ( больше 0,5В)
б) в местах соединений, выполненных с помощью металлов или сплавов разного состава
в) в изделиях, изготовленных из одного металла, но находящегося в различных состояниях ( отжиг, закалка и др.), или имеющего другие неоднородности
г) в электролитах, окислительные ионы которых более положительны, чем металл изделия, например железо или алюминий в растворах медных солей. В этом случае контакт возникает в результате отложения металлической меди ( из раствора) на стальном изделии.
Потенциалы металлов в различных электролитах не одинаковы. Поэтому интенсивность контактной коррозии зависит не только от природы контактирующих металлов , но и от электролита. В табл. 1.3 приведены знаяения потенциалов некоторых металлов в типичных электролитах.

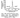
Коррозия наиболее интенсивна вблизи контакта и ослабевает по мере удаления от места контакта.
Характерное распределение плотности тока для пары медь - железо в зависимости от расстояния от места контакта показано на рис. 1. 26.
Характерное распределение плотности тока для пары медь - железо в зависимости от расстояния от места контакта показано на рис. 1. 26.
Благодаря электропроводности раствора контактная коррозия может возник-нуть, если металлы непосредственно и не соприкасаются, а расположены на некотором (меньше предельного) расстоянии друг от друга. Например, Г. Уллиг считает, что в водопроводной воде предельное расстояние между медью и железом составляет 0,5 см, а в морской воде — несколько дециметров.
Большое значение имеет также соотношение площа- дей анода и катода в контактной паре. Увеличение площа- ди катода облегчает протекание катодных процессов, деполяризацию, усиливая интенсивность контактной коррозии. Зависимость скорости анода (А), находящегося в контакте с более благородным метал- лом (В), от соотношения их площадей может быть вы- ражена следующим уравнением [22]
р — проницаемость (скорость коррозии) контактируемого ме- талла; — анода; р0— проницаемость этого металла без контакта; В — площадь более благородного металла (катода); А — площадь металла (анода).
При равных площадях анода и катода нежелатель- ные контакты определяются разницей потенциалов и данном электролите.
Большое значение имеет также соотношение площа- дей анода и катода в контактной паре. Увеличение площа- ди катода облегчает протекание катодных процессов, деполяризацию, усиливая интенсивность контактной коррозии. Зависимость скорости анода (А), находящегося в контакте с более благородным метал- лом (В), от соотношения их площадей может быть вы- ражена следующим уравнением [22]
р — проницаемость (скорость коррозии) контактируемого ме- талла; — анода; р0— проницаемость этого металла без контакта; В — площадь более благородного металла (катода); А — площадь металла (анода).
При равных площадях анода и катода нежелатель- ные контакты определяются разницей потенциалов и данном электролите.
