Кинетика электрохимической коррозии металлов.
Кинетика процесса электрохимической коррозии металлов, то есть его скорость, определяется комплексом факторов. Эти факторы влияют на скорость протекания анодных и катодных процессов на поверхности металла, что непосредственно отражается на изменении двух ключевых параметров: силы коррозионного тока и электродных потенциалов.
Ключевой фактор: Поляризация электродов
Самым важным фактором, контролирующим скорость коррозии, является поляризация. Это явление представляет собой изменение значений начальных (равновесных) потенциалов электродов (анода и катода) при замыкании цепи в коррозионном элементе и протекании тока.
- Результат поляризации: Это изменение потенциалов приводит к значительному снижению движущей силы коррозионного элемента и, как следствие, к уменьшению силы коррозионного тока и скорости коррозии. Фактически, поляризация является естественным "тормозом" процесса.
- Виды поляризации:
- Анодная поляризация: Поскольку при анодном процессе (растворении металла) происходит сдвиг потенциала в сторону положительных значений, то повышение потенциала анода относительно его начального значения и характеризует анодную поляризацию. Она может быть вызвана затруднениями в стадиях ионизации металла или образованием пассивных пленок.
- Катодная поляризация: Это понижение потенциала катода (сдвиг в сторону отрицательных значений). Она возникает из-за ограниченной скорости доставки окислителя (например, кислорода) или замедленной стадии разряда ионов на поверхности катода.
Явление, противоположное поляризации и препятствующее поляризуемости электродов, называется деполяризацией. Деполяризация увеличивает скорость коррозионного процесса, снимая ограничения.
- Катодная деполяризация: Наиболее распространенный вид. Это ускорение катодной реакции, например, за счет интенсивной подачи кислорода (аэрации) или присутствия сильных окислителей. Именно деполяризаторы (кислород, ионы водорода) часто являются главной причиной интенсивной коррозии.
- Анодная деполяризация: Устранение факторов, замедляющих анодный процесс (разрушение пассивной пленки, комплексообразование).
---
Анодная поляризация — это повышение потенциала анода (участка растворения металла) в положительную сторону, что приводит к торможению процесса коррозии. Она возникает по нескольким ключевым причинам:
Перенапряжение процесса ионизации металла:
- Механизм: Ситуация, когда выход электронов из металлической решетки происходит быстрее, чем непосредственный переход ионов металла в раствор. Это создает временный дисбаланс.
- Результат: Отрицательный заряд металла в двойном электрическом слое уменьшается, что вызывает сдвиг потенциала анода в сторону положительных значений. Это кинетическое препятствие для растворения.
- Механизм: На поверхности металла (анода) спонтанно или под действием среды образуются плотные, нерастворимые в электролите пленки (оксиды, фосфаты, хроматы). Эти пленки препятствуют протеканию процесса ионизации металла, блокируя контакт с раствором.
- Результат: Металл под пленкой приобретает значительно более положительный (благородный) потенциал, переходя в пассивное состояние. Это мощнейший фактор торможения коррозии (например, пассивация нержавеющей стали, алюминия, титана).
- Механизм: В прианодном слое раствора происходит накопление положительных ионов металла, перешедших в раствор. Если их отвод из этой зоны вглубь раствора затруднен (медленная диффузия или конвекция), концентрация у поверхности растет.
- Результат: Повышение концентрации собственных ионов смещает равновесие и затрудняет дальнейший переход ионов из решетки, что также приводит к положительному сдвигу потенциала.
Катодная поляризация — это понижение потенциала катода (участка восстановления окислителя) в отрицательную сторону. Она обусловлена сложностью и ступенчатым характером катодного процесса восстановления ионов-деполяризаторов (H⁺, O₂).
Основные лимитирующие стадии (причины замедления):
- Диффузионная стадия: Восстанавливающимся ионам или молекулам кислорода необходимо диффундировать через толщу раствора, чтобы подойти к поверхности катода. При медленной подаче (например, в спокойном растворе или вязкой среде) эта стадия лимитирует весь процесс.
- Стадия разряда (перенапряжение): Даже достигнув поверхности, частицы (например, ионы H⁺) должны подвергнуться дегидратации (потерять сольватную оболочку) и непосредственно принять электрон с поверхности металла. Энергетический барьер этой электрохимической реакции создает перенапряжение разряда.
- Стадия отвода продуктов: Образовавшиеся продукты (например, газ H₂ или OH⁻-ионы) должны удаляться от поверхности, иначе они блокируют активные центры.
Катодная поляризация, проявляющаяся в сдвиге потенциала катода в отрицательную сторону, является естественным тормозом для электрохимической коррозии. Её интенсивность и, следовательно, степень замедления коррозии определяются двумя основными группами факторов:
1. Перенапряжение катодной реакции (кинетический контроль)
Этот фактор связан с энергетическими барьерами самой электрохимической реакции на поверхности катода.
- Механизм: Перенапряжение возникает, когда восстановление (разряд) деполяризатора происходит медленнее, чем поступление электронов с анода через металл. В результате электроны скапливаются у катода, что и вызывает сдвиг его потенциала в отрицательную сторону.
- Типы перенапряжения:
- При водородной деполяризации наблюдается перенапряжение водорода (ηн). Его величина сильно зависит от материала катода (высокое на свинце, олове; низкое на платине, палладии).
- При кислородной деполяризации возникает перенапряжение восстановления кислорода (ηо₂). Этот процесс также имеет высокое перенапряжение на многих металлах.
Этот фактор связан с ограничениями в поставке реагирующих веществ к поверхности катода.
- Механизм: Замедленность диффузии деполяризатора (ионов H⁺ или молекул O₂) из объемного электролита к поверхности катода приводит к их истощению в прикатодном слое. В этой зоне относительно увеличивается концентрация «свободных» электронов, что и делает потенциал катода более отрицательным.
- Примеры: Коррозия в спокойных, вязких растворах или под плотными отложениями, где доступ окислителя затруднен. Это явление лежит в основе работы некоторых ингибиторов коррозии, которые создают на поверхности барьерные пленки, затрудняющие диффузию.
Все факторы, способствующие как катодной, так и анодной поляризации, в конечном итоге уменьшают силу коррозионного тока и, следовательно, скорость процессов электрохимической коррозии. Они повышают коррозионную стойкость металла в электролите, создавая кинетические препятствия для протекания анодного и катодного процессов.
Наиболее важным является перенапряжение водорода (катодного процесса), определяющее, по существу, кинетику электрохимической коррозии. Чем больше перенапряжение водорода, тем более затруднено протекание процесса коррозии и тем меньше, следовательно, скорость коррозии металла.
Значение перенапряжения зависит от природы металла, состояния его поверхности, соотношения размеров площадей анода и катода и других факторов.
Процессы, протекающие с водородной деполяризацией — разрядом ионов водорода на катоде — проходят следующие стадии:
б) дегидратация
H2O → H+ H2O
в) восстановление (разряд) ионов водорода
H+ e- → H
г) соединение атомов водорода в молекулу
H + H → H2
д) ассоциация молекул водорода, образование пузырьков газа и их выделение
H2 + H2 + H2+... → H2↑
Также сложны катодные процессы ионизации кислорода, протекающие по-разному в кислых и щелочных средах (или в нейтральных средах). В первом случае образующиеся ионы кислорода взаимодействуют с ноном водорода кислоты, во втором — с молекулами воды.
Ниже приводится схема процесса ионизации кислорода в кислой и щелочной средах:

n=a+blg ik, v=a'+b'lg ik
где п — перенапряжение водорода; v — перенапряжение ионизации кислорода; ik — плотность катодного тока; а, а', b, b' — постоянные.
Константы а и а' зависят от природы и кристаллического строения металла — катода, состояния его поверхности, температуры, состава электролита и других факторов. Константы b и b' от материала не зависит. Значения перенапряжения водорода и ионизации кислорода для различных металлов, вычисленные при плотности катодного тока 10 А/м2, приводятся ниже

Поляризационные кривые являются основным экспериментальным инструментом в электрохимической коррозии. С помощью этих кривых можно:
- Определить характер электрохимической коррозии металлов (активный, пассивный, склонный к питтингу).
- Установить кинетику процесса, то есть количественно оценить скорость коррозионного разрушения.
- Исследовать влияние различных факторов на протекание коррозии (состав среды, температура, наличие ингибиторов, потенциал).
- Определить такие ключевые параметры, как потенциал коррозии, плотность тока коррозии, области пассивности и потенциал пробоя.
Построение поляризационных кривых: принцип и уравнения
Поляризационные кривые строятся в координатах: ток (плотность тока) — потенциал. Именно эти показатели являются основными, контролирующими кинетику коррозионного процесса.
- Ось ординат (Y): Сила тока (I) или, чаще, плотность тока (i), выраженная в А/см². Эта величина прямо пропорциональна скорости коррозии по закону Фарадея.
- Ось абсцисс (X): Электродный потенциал (E), измеренный относительно электрода сравнения (например, хлорсеребряного). Сдвиг потенциала отражает степень поляризации электрода.


Поляризационная диаграмма окисления металла: а – анодная кривая; К – катодная кривая; α – угол, характеризующий перенапряжение катодного процесса.
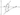
Когда скорость процессов окисления металла и восстановления окислителя будут равны, устанавливается
стационарное состояние, при котором iₐ= iₕ, процесс протекает с некоторой постоянной скоростью, а значение потенциала электрода соответствует значению стационарного потенциала (ȹс).
С помощью поляризационных кривых можно установить, что коррозионный процесс зависит от следующих основных факторов:
1. От разности между равновесными потенциалами металла (ȹᴹᵉравн) и окислителя (фᴼᵏравн) в случае, если кинетика обоих процессов (анодного и катодного) одинакова.
2. От угла наклона поляризационных кривых, который характеризует перенапряжение окислительно-восстановительного процесса.
В катодном процессе перенапряжение водорода обратно пропорционально тангенсу угла наклона поляризационных кривых (рис1)
По катодной кривой можно судить о влиянии, например, состояния поверхности металла на перенапряжение водорода. И, соответственно, на скорость коррозии. Так, катодные кривые для технического и чистого цинка имеют различные углы наклона. Для чистого цинка угол наклона меньше, следовательно, перенапряжение катодного процесса больше, а скорость коррозии меньше; для технического цинка, с более развитой неоднородной поверхностью, — перенапряжение меньше, и процесс коррозии протекает с большей скоростью.
3. От концентрации ионов новой окислителя электролита или их активности в процессах с водородной деполяризацией (рис. 2). При меньшей концентрации ионов водорода, например в 2%-ной серной кислоте, потенциал окислителя имеет значение фок; в 10%-ной кислоте он положительнее (ȹ'ок.). Им соответствуют две катодные кривые (2 и 3) и разные значения стационарных потенциалов (ȹс и ȹ'с.). Из рисунка видно, что процесс коррозии в более концентрированной кислоте протекает с большей скоростью, так как при этом сила коррозионного тока возрастает от ia, до і'a
4. От контакта между разнородных металлов в одном электролите (рис. 1.13). Поляризационные кривые характеризуют взаимное влияние металлов на процесс
коррозии и показывают, что металл с более отрицательным потенциалом полностью защищает от коррозии металл с более положительным потенциалом.
Если эти металлы не контактируют, то они окисляются со скоростью, определяемой соответствующими анодными кривыми и силой тока і¹а и і²a в стационарных условиях. Перенапряжение катодного процесса на них одинаково: на металле с более положительным потенциалом (Меп) перенапряжение больше и угол наклона катодной кривой меньше, чем для металла с более отрицательным потенциалом (МеI).
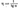
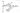
Такое замедление процесса коррозии одного из металлов при их контакте используется в качестве защиты от коррозии и называется протекторной защитой. По отношению к стали эффективными протекторами являются, например, цинк и магний. По мере их разрушения они заменяются новыми, а стальные конструкции сохраняются.
С помощью поляризационных кривых можно установить и многие другие факторы, влияющие на коррозионный процесс в зависимости от условий, в которых он протекает.
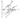
Рис.3. Поляризационная диаграмма совместного окисления двух различных металлов в одном электро-лите (окислителе).
На рис.4 представлены схематическая потенциостатическая поляризационная диаграмма, раскрывающая переход металла из одного состояния в другое в процессе коррозии.
Область Фравн — Фп (потенциал начала пассивации) отражает активное состояние металла, корродирующего со скоростью, соответствующей силе анодного тока, по значению iп (в стационарных условиях).
Область Фп - Фпп (потенциал полной пассивации) соответствует процессу пассивации, переходу металла в пассивное состояние, т. е. неустойчивой пассивности, когда сила анодного тока уменьшается, процесс коррозии замедляется, но еще не прекращается.
В области устойчивого пассивного состояния сила коррозионного тока постоянна и минимальна (Iпп), хотя сдвиг потенциала в положительную сторону продолжается от Фпп до Факт потенциала соответствующего переходу металла вновь в активное состояние

Рис.4 Общий вид потенциалоэлектрической поляризационной диаграммы.
4OH¯ - 4e→ O2 + 2H2O
Участок кривой Факг – Фо2 соответствует, таким образом, области перепассивации и возрастанию скорости коррозионного процесса.Такого типа кривые характеризуют различную способность металлов к пассивации. На рис.5 представлены потенциалостатические поляризационные кривые железа и хрома в 1 н. серной кислоте при обычной температуре. Они показывают, что область пассивации хрома начинается при более отрицательных значениях потенциала (~ -0,1 В), а для железа только при +0,5 В. Область перепассивации железа обусловлена выделением кислорода, для хрома — образованием растворимых в кислоте хроматов.
Поляризационные диаграммы для различных усло-вий электрохимической коррозии металлов.
Поляриза-ционные кривые можно получать гальваностатическим или потенциостатическим методами. В первом случае фиксируется ток и измеряется потенциал; во втором — замеряется ток при установившихся значениях потен-циала. Изображение поляризационных диаграмм может отличаться от приведенных выше, если анодный и ка-тодный токи (I) откладываются в одном направлении по оси абсцисс, а потенциал (Е) — по оси ординат (рис. 6). Поэтому и приводимые ниже примеры по-ляризационных кривых не идентичны.
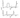
Рис.5. Потенциостатические поляризационные кри-вые для железа (а) и хрома (б) в 1 н. серной кислоте: 1 и 2 — области перепассивации
меньшей концентрации кислорода (пунктирная кривая, i'корр).
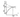
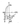
Рис. 6. Поляризационная диаграмма коррозии
ЕᴼẠ и Еᴼк — начальные потенциалы металлов — входа и окислителя — катода; Ех — общей (стационарной) потенциал коррозии; iкорр— максимальный ток коррозии.
Рис.7. Схематическая поляризационная диаграмма
коррозии железа в растворах солей [1, с. 76].

Рис. 1.18. Поляризационные кривые, измеренные в 0,1 н. серной кислоте на стали 1Х13 (а) и на сплаве с 27% хрома (б).
1, 3 — анодная и катодная кривые, полученные при 50°С, 2, 4 — то же при 80°С (по Я. М. Колотыркину и Г. М. Флорианович)Весьма наглядно характеризуется поляризационными кривыми влияние растворенного кислорода на коррозионную углеродистой стали (Ст3) в морской воде (рис. 1.20).
